Gérer la maladie de Parkinson

Les traitements
Au cours des 30 dernières années, grâce à une meilleure compréhension des processus pathologiques sous-jacents, le traitement de la maladie de Parkinson a fait des progrès remarquables.
Si aucun traitement ne permet de guérir, ils contribuent tous au contrôle des symptômes et à l’amélioration de la qualité de vie.
La prise en charge thérapeutique de la maladie de Parkinson est complexe: diverses approches (médicamenteuses, assistées par un dispositif, chirurgicales, rééducatives,…), divers modes d’administration (oral, percutané, sous-cutané,…) et de multiples dosages.
Cette complexité est une richesse qui permet une approche personnalisée adaptée à l’évolution de la maladie.
La L-dopa demeure le médicament principal au début de la maladie. Il est souvent combiné avec d’autres produits pour maximiser son efficacité tout en maintenant des doses modestes et préservant la tolérance à long terme.
Au fur et à mesure de l’évolution de la maladie, les thérapies assistées par dispositif (pompes) ou les approches chirurgicales (DBS) peuvent être envisagées.
Le choix du traitement dépend de nombreux facteurs individuels, tels que l’âge, les symptômes, les besoins spécifiques du patient ou encore la gestion des comorbidités (autres maladies qui affectent le patient) : une décision qui incombe au médecin et nécessite une grande rigueur dans la prise des médicaments. L’automédication est à proscrire !
En plus des médicaments, la rééducation physique joue un rôle crucial. La pratique d’une activité sportive adaptée fait partie des traitements non-médicamenteux performants.
L’information et l’éducation sont également essentielles pour garantir l’implication active du patient comme de ses proches et maintenir ainsi au mieux la qualité de vie.
Traitements médicamenteux
La Levodopa (L-dopa)
La L-dopa est actuellement le traitement de référence.
Cette molécule, habituellement bien tolérée, est transformée en dopamine par le cerveau lui-même.
En début de traitement, le patient peut éprouver de légers étourdissements ou des nausées qui disparaissent presque toujours après réduction de la dose. Très occasionnellement, sans danger, les urines peuvent prendre une coloration brunâtre. Au fur et à mesure de l’évolution de la maladie, la réponse favorable au traitement a tendance à s’estomper, donnant lieu à des fluctuations de la mobilité (effets « on/off ») et à des mouvements involontaires (dyskinésies, dystonies).
Le retard de vidange gastrique et les problèmes de déglutition contribuent de manière significative aux fluctuations de la mobilité.
À ce stade, il devient de plus en plus difficile d’optimiser la médication, malgré la possibilité de fractionner le traitement (prises multiples de doses plus faibles) ou de l’associer à d’autres médicaments. Des injections sous-cutanées d’apomorphine peuvent alors éventuellement être envisagées pour gérer par intermittence les moments « off » prévisibles (voir « Les agonistes de la dopamine »). L’amantadine, qui n’est plus délivrée en Belgique mais peut être importée des pays voisins, peut s’avérer utile pour gérer les dyskinésies (voir « L’amantadine »).
Lorsque cette phase avancée a de plus en plus de répercussions sur la qualité de vie, un traitement continu peut être envisagé (voir « Thérapies assistées par un dispositif et les traitements chirurgicaux »).Les agonistes de la dopamine
Ces médicaments imitent l’effet de la dopamine en stimulant directement ses récepteurs. Ils n’augmentent donc pas la quantité de dopamine mais assurent une stimulation continue des récepteurs dopaminergiques, facilitant ainsi la conduction de l’influx nerveux.
Il peuvent être utilisés en monothérapie ou en association avec la L-dopa et sont proposés sous différentes formes d’administration : orale, transdermique (patch) ou injectable (stylo d’apomorphine).Il en existe 2 types :
-les dérivés de l’ergot de seigle (bromocriptine, cabergoline, pergolide).
Ces alcaloïdes comprennent également des produits destinés à bloquer la lactation des femmes et à traiter le gigantisme.
Les 1ères études ont révélé que l’administration précoce d’une association de L-dopa et d’un agoniste dopaminergique pouvait retarder la survenue des fluctuations de la mobilité et des dyskinésies.-les non-ergolines (ropinirole, pramipexole, apomorphine), plus récents et désormais préférés car ils présentent un profil de tolérance plus favorable malgré une tendance plus marquée à augmenter la somnolence diurne.
L’instauration d’un traitement par agonistes dopaminergiques doit se faire progressivement et avec prudence, afin de limiter la survenue de nausées, de vomissements ou parfois d’hypotension orthostatique (environ 10 % des cas). Ces médicaments peuvent également entraîner une somnolence excessive ou des troubles psychiatriques tels que confusion, hallucinations, comportements impulsifs ou conduites addictives. La plupart de ces effets indésirables ont toutefois tendance à s’atténuer avec le temps ou peuvent être contrôlés par des mesures thérapeutiques adaptées.
Une approche pluridisciplinaire est souhaitable pour contourner ces effets secondaires.Pour l’apomorphine, une technique spécifique par voie sous-cutanée permet d’éviter la destruction hépatique importante et immédiate en cas de prise orale. Ceci en fait un traitement de secours et de réserve lorsque tous les autres traitements se révèlent insuffisants pour une qualité de vie suffisante.
L’injection intermittente grâce au stylo est utilisée pour lever rapidement les épisodes « off ». Une perfusion continue par pompe permet une délivrance régulière de la molécule pendant la journée, avec possibilité d’ajuster par des bolus (voir « Thérapies assistées par un dispositif et les traitements chirurgicaux : vue d’ensemble »).
Cette approche stabilise les fluctuations motrices, augmente le temps passé en période « on », réduit les dyskinésies, et peut même améliorer les troubles du sommeil lorsqu’elle est administrée la nuit.
Les effets secondaires, au long terme, s’illustrent surtout en réactions cutanées locales (rougeurs, nodules, indurations).
L’amantadine
L’action bénéfique de ce médicament antiviral dans la maladie de Parkinson a été fortuitement découverte dans les années 1960 lorsqu’une patiente atteinte de la maladie de Parkinson constata une amélioration de ses symptômes parkinsoniens durant son traitement grippal.
Son rôle principal aujourd’hui est le traitement des dyskinésies, ces mouvements involontaires apparaissant fréquemment sous L-dopa.
L’amantadine agit selon un double mécanisme :
– elle augmente la disponibilité de la dopamine (en favorisant sa libération et en bloquant sa recapture)
– elle exerce une action antiglutamatergique (antagoniste des récepteurs NMDA), ce qui explique son effet antidyskinétique.Indisponible en Belgique depuis 2011, elle peut encore être importée d’autres pays voisins.
Le traitement débute généralement avec un délai d’action de quelques jours et son efficacité peut s’atténuer avec le temps.Concernant la tolérance, l’amantadine peut provoquer des effets secondaires tels que nausées, insomnie (si prise tard le soir), œdèmes des jambes ou livedo reticularis (aspect marbré bleuâtre de la peau). Ces effets sont bénins mais parfois gênants.
Peuvent également survenir, notamment chez la personne âgée, des effets neuropsychiatriques (anxiété, confusion, hallucinations, troubles de l’humeur) qui justifient une surveillance attentive.Les anticholinergiques
Les anticholinergiques de synthèse sont apparus dans les années 50, offrant une approche thérapeutique plus standardisée de la maladie de Parkinson qui, jusqu’à la fin de la seconde guerre mondiale n’avait pour seul recours médicamenteux que l’extrait de racine de belladone (atropine et scopolamine).
Leur action n’est pas directement en lien avec la dopamine : comme le terme « anticholinergique » l’indique, ils réduisent la relative prédominance de l’acétylcholine sur la dopamine, contribuant ainsi à rétablir un certain équilibre entre les deux neurotransmetteurs, mais à un niveau inférieur à celui des traitements dopaminergiques.Historiquement prescrits pour le tremblement et la rigidité, leur usage s’est fortement restreint. Les médecins sont aujourd’hui plus réticents à les prescrire en raison de leurs nombreux effets secondaires. D’autant que dans de nombreux cas, tremblement et rigidité peuvent désormais être gérés par des médicaments plus efficaces et mieux tolérés, notamment la L-dopa, les agonistes dopaminergiques ou encore l’amantadine.
Cependant, les anticholinergiques conservent certaines indications spécifiques comme le tremblement de repos résistants à la L-dopa, un trouble de la déglutition (difficulté à gérer la salive) ou une sudation excessive.
Leur utilisation nécessite des précautions particulières chez les patients atteints de glaucome, avec surveillance ophtalmologique rigoureuse, ainsi que chez ceux à risque d’arythmies cardiaques, de constipation ou de rétention urinaire. Des effets cognitifs et psychiatriques tels que confusion, troubles de la mémoire et hallucinations sont également rapportés.
Ces médicaments sont généralement mieux tolérés par les jeunes patients dont le profil cognitif et la santé générale limitent le risque d’effets indésirables. En revanche, sur tout au-delà de 65 ans, ils sont à éviter ou à utiliser avec grande prudence.
Les inhibiteurs
Une partie des traitements antiparkinsoniens repose sur l’inhibition d’enzymes qui dégradent la dopamine ou la L-dopa, afin de prolonger et renforcer leur action. Deux grandes familles existent :
– les inhibiteurs de la COMT (Catéchol-O-Méthyl-Transférase) :
L’enzyme COMT dégrade la L-dopa dans le sang, si bien qu’à peine 1 % atteint le cerveau. L’action des inhibiteurs de la COMT limitent la perte et augmentent donc la proportion de L-dopa disponible ce qui prolonge son effet. Les études montrent une réduction d’environ 10 % de la dose de L-dopa nécessaire et une amélioration équivalente des périodes « off ». Seul l’entacapone est disponible en Europe, la tolcapone ayant été retirée en raison d’une toxicité hépatique.
Les effets indésirables éventuels sont des dyskinésies, diarrhées tardives et coloration brunâtre des urines (sans gravité).– les inhibiteurs de la MAO-B (MonoAmine-Oxydase B) :
Ces inhibiteurs, apparus dans les années 80 dans le traitement de la maladie de Parkinson, agissent directement dans le cerveau en bloquant l’enzyme MAO-B, responsable de la dégradation de la dopamine. Leur utilisation permet de prolonger l’effet de la dopamine endogène et de la L-dopa administrée. Ils sont surtout utiles en début de maladie, avec un effet démontré dans plusieurs essais (DATATOP, SELEDO), pouvant retarder le recours à la L-dopa d’environ 9 mois. Leur intérêt persiste aussi en association aux stades plus avancés, notamment pour réduire les fluctuations motrices. Ils sont globalement bien tolérés. Les effets indésirables sont similaires à ceux de le L-dopa.Ainsi, qu’ils agissent en périphérie (COMT) ou au niveau cérébral (MAO-B), ces inhibiteurs partagent le même principe d’action qui optimise l’utilisation de la dopamine et prolonge les effets de la L-dopa.
Thérapies assistées par un dispositif et Traitements chirurgicaux
Thérapies assistées par un dispositif
Vue d'ensembleLes thérapies par pompe représentent une avancée majeure dans la prise en charge des formes avancées de la maladie de Parkinson. Ces thérapies offrent une alternative efficace pour améliorer la qualité de vie lorsque les traitements oraux ne permettent plus un contrôle optimal des symptômes.
Elles permettent l’administration continue de médicaments (principalement L-dopa) afin de maintenir une concentration stable dans le sang, ce qui réduit les fluctuations motrices et les périodes OFF imprévisibles.
L’administration en continu s’avère également utile en cas de déclin cognitif.En Belgique, trois types de pompes sont actuellement accessibles sous conditions : Duodopa®, Lecigimon® et ProDuodopa®.
La pompe à apomorphine, administrée en sous-cutanée, par perfusion continue constitue une autre alternative pour les patients parkinsoniens avancés, en particulier lorsqu’une SCP (voir « Traitements chirurgicaux ») n’est pas réalisable. Son utilisation en Belgique demeure marginale, notamment en raison de l’absence de commercialisation du dispositif sur le territoire. Dans la pratique, l’accès peut se faire via des préparations magistrales hospitalières ou, dans certains cas spécifiques, par un approvisionnement transfrontalier encadré. Il arrive donc que cette pompe soit utilisée comme solution transitoire en attendant la mise en place d’une SCP.
Alternative à l’injection intermittente grâce au stylo (voir « Les agonistes de la dopamine »), cette perfusion continue par pompe permet une délivrance régulière de la molécule pendant la journée, avec possibilité d’ajuster par des bolus.
Cette approche stabilise les fluctuations motrices, augmente le temps passé en période « on », réduit les dyskinésies, et peut même améliorer les troubles du sommeil lorsqu’elle est administrée la nuit.
Les effets secondaires, au long terme, s’illustrent surtout en réactions cutanées locales (rougeurs, nodules, indurations). Les effets systémiques (nausées, hypotension orthostatique, hallucinations) sont contrôlables par des ajustements thérapeutiques.Thérapies assistées par un dispositif - Les pompes à L-Dopa
Duodopa®, Lecigimon® et ProDuodopa®Duodopa et Lecigimon sont dites « thérapies par pompe intestinale ».
L’avantage de ces pompes est l’administration du gel contenant les principes actifs directement dans l’intestin grêle, via la paroi abdominale et l’estomac à l’aide d’une sonde.
En délivrant le médicament directement dans l’intestin, on peut contourner les effets négatifs d’un ralentissement de la vidange gastrique et des problèmes de déglutition.
Pour permettre une administration continue du gel, une pompe électronique externe est fixée à la sonde.Il existe des sacs et vêtements adaptés permettant de dissimuler la pompe en toute sécurité.
Ces traitements nécessitent une intervention chirurgicale préalable et une surveillance technique régulière.
Ce sont les complications mécaniques (déplacement/occlusion sonde) qui sont l’effet secondaire désagréable le plus fréquent. On note également des infections locales et des neuropathies (surtout en cas d’usage prolongé ou carence en vitamines).Produodopa propose une alternative non invasive par voie sous-cutanée dont les effets indésirables sont essentiellement cutanés (érythème, nodule, œdème, cellulite, abcès).
Cette thérapie requiert également une surveillance technique régulière.Pour pouvoir bénéficier du remboursement de ces thérapies, le patient doit d’abord être soumis à une évaluation approfondie avec des critères stricts.
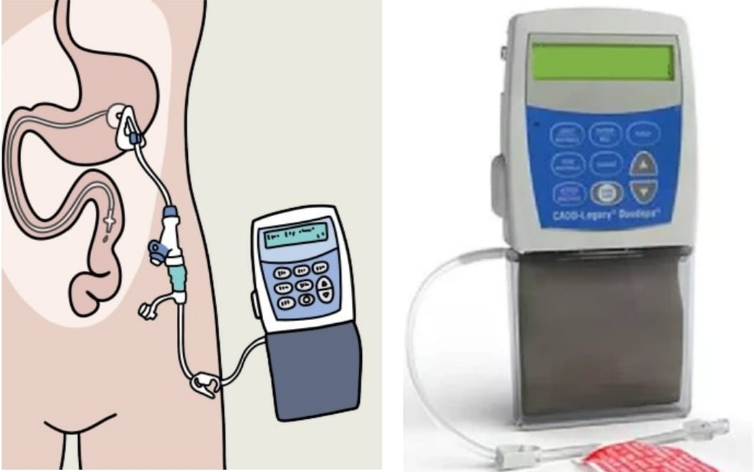
Duodopa – Pompe à gel intestinal
Duodopa, traitement disponible en Belgique depuis 2007, reste la solution standard par voie intestinale.
Le gel intestinal, stocké dans une cassette en plastique, contenant de la L-Dopa et de la carbidopa, est administré en continu directement dans le jéjénum via une fine sonde insérée via la paroi abdominale et gastrique.La pompe, portée près du corps, permet de délivrer le traitement de manière contrôlée tout au long de la journée (généralement 16h à 24h). Cette administration continue permet d’améliorer les symptômes moteurs (réduction des « OFF », des dyskinésies et du « freezing » ; amélioration de la marche).
Lecigimon – Pompe à gel intestinal enrichi
Lecigimon est disponible en Belgique depuis 2022. La principale différence avec Duodopa réside dans l’ajout d’entacapone dans le gel Lecigimon.
L’entacapone est un inhibiteur spécifique et réversible qui agit dans les tissus périphériques. En inhibant l’activité de l’enzymze COMT (voir « Les inhibiteurs »), il permet à une plus grande quantité de L-Dopa d’atteindre le cerveau. Cela permet de réduire les fluctuations de symptômes qui peuvent survenir en fin de dose, lorsque l’effet du médicament diminue.L’ajout d’entacapone permet également de réduire davantage la dose quotidienne de L-Dopa. Grâce à l’administration continue d’une petite quantité de médicament tout au long de la journée, ces systèmes permettent de maintenir une concentration constante dans le sang, ce qui contribue à diminuer l’incidence des effets secondaires moteurs indésirables.
Les cartouches de Lecigimon sont plus petites que celle de Duodopa mais sont suffisantes grâce à l’ajout d’entacapone.
En général, une dose initiale est administrée le matin pour atteindre rapidement la concentration souhaitée dans le sang. Ensuite, une dose continue est automatiquement délivrée tout au long de la journée. Généralement déconnectée la nuit, la thérapie peut toutefois être poursuivie la nuit si nécessaire.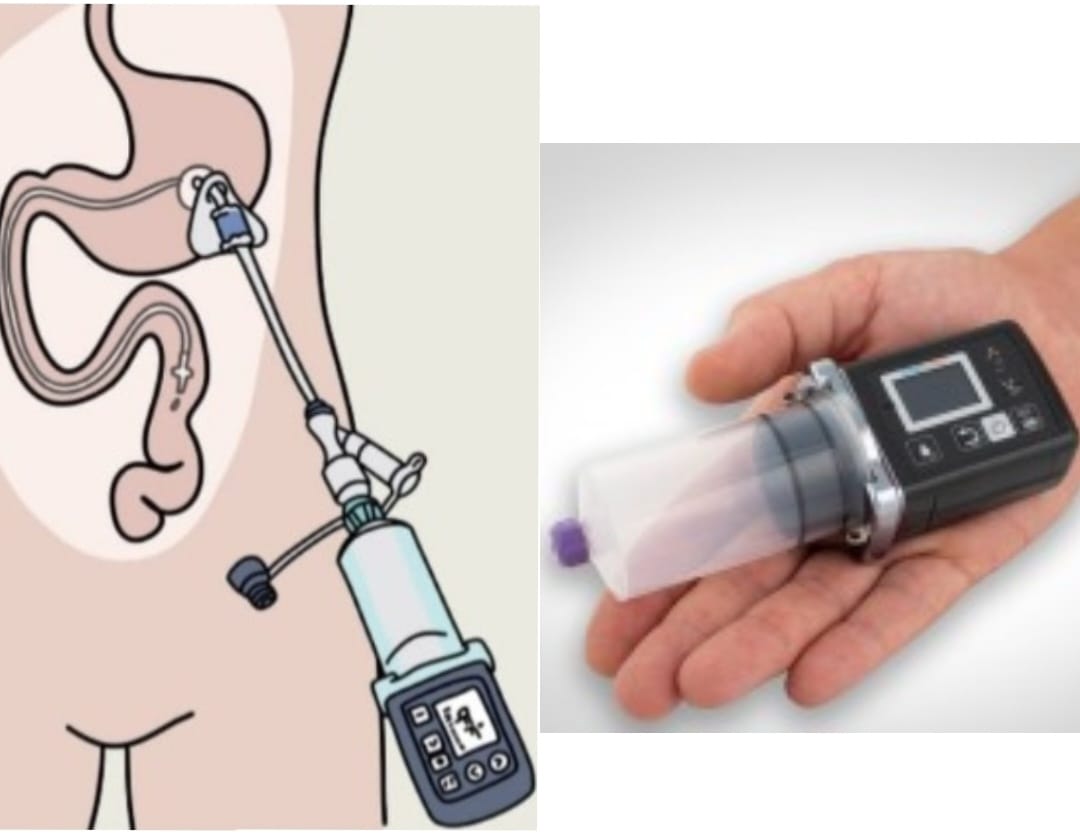
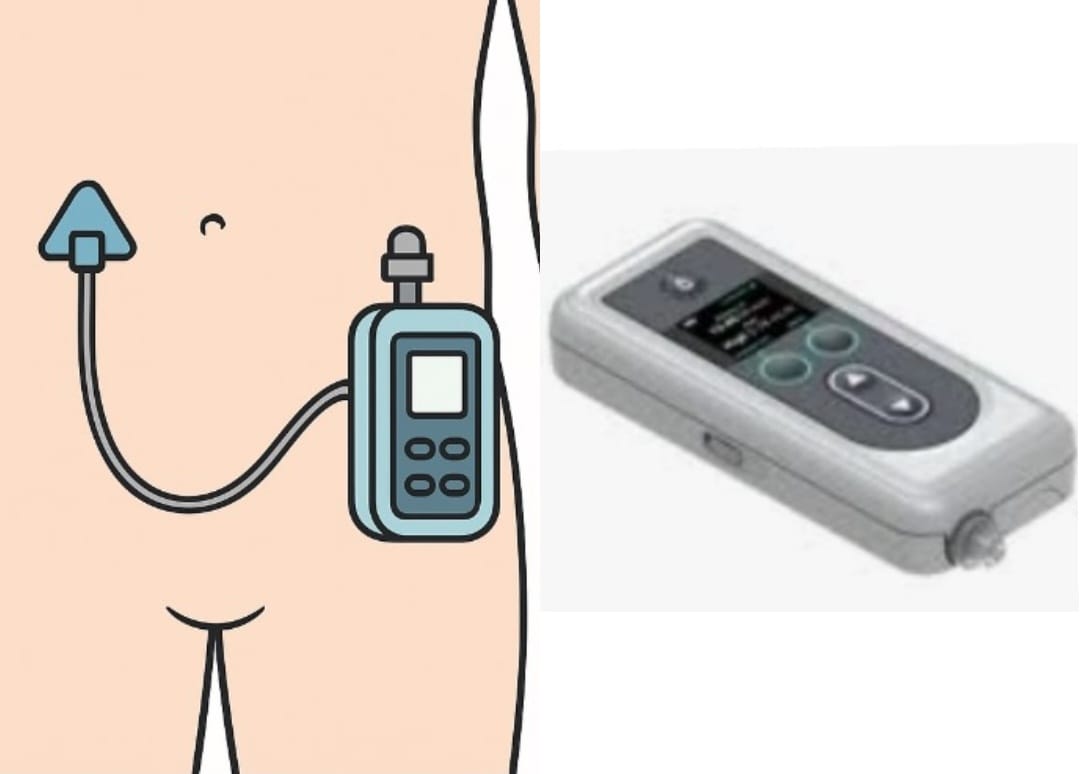
ProDuodopa – Pompe sous-cutanée
Produodopa, disponible en Belgique depuis 2024 seulement, est une thérapie innovante administrée par voie sous-cutanée.
Elle contient 2 composants actifs : la foslevodopa et la foscarbidopa, qui, regroupés dans une flapule de solution forment le ProDuodopa. Dans l’organisme, la foslevodopa est transformée en dopamine alors que la foscarbidopa améliore les effets de la foslevodopa et en réduit les effets indésirables.Le traitement est ajusté individuellement avec possibilité de programmer différents dosages selon les moments de la journée. Les sites d’injections sont variés (abdomen, bras, cuisses, flancs). La canule est changée tous les 2 à 3 jours.
La pompe est prévue pour un traitement de 24h, selon la prescription du neurologue. Légère, elle peut se porter en bandoulière ou à la ceinture. Le traitement peut être stoppé pour une activité précise (douche, examen,…) mais s’il est stoppé au moins 1 heure, la pompe devra être arrêtée et un nouveau dispositif devra être repositionné.
ProDuodopa ne nécessite pas de chirurgie abdominale. Moins invasive, cette pompe est adaptée aux patients ne pouvant bénéficier des pompes intestinales ni subir de traitement chirurgical.
Traitements chirurgicaux - Les chirurgies lésionnelles
Thalamotomie, Pallidotomie et SubThalamotomieLes chirurgies lésionnelles, apparues dans les années 1950, ont constitué les premières approches chirurgicales efficaces pour traiter les troubles moteurs de la maladie de Parkinson. Elles consistaient à détruire de manière ciblée et stéréotaxique certaines structures cérébrales impliquées dans la genèse des symptômes moteurs.
Avec l’introduction de la L-dopa dans les années 1970, ces interventions ont connu un recul marqué, avant de bénéficier d’un renouveau transitoire dans les années 1980.
Ensuite, à partir des années 1990, elles ont été progressivement supplantées par la stimulation cérébrale profonde (SCP) qui offre une alternative réversible et ajustable aux traitements destructifs.Les chirurgies lésionnelles consistent à créer une lésion permanente et localisée dans une région cérébrale hyperactive, afin de rééquilibrer l’activité des circuits moteurs.
Les principales cibles chirurgicales sont :
- le noyau ventral intermédiaire du thalamus (VIM), destiné au traitement du tremblement
- le globus pallidus interne (GPi), ciblé pour la rigidité et les dyskinésies
- et plus rarement le noyau sous-thalamique (NST).
Plusieurs techniques peuvent être utilisées :
- Thermocoagulation stéréotaxique : destruction du tissu ciblé par élévation de température (électrode chauffée)
- Radiochirurgie (Gamma Knife®) : destruction par irradiation focalisée, sans ouverture chirurgicale
- Ultrasons focalisés de haute intensité (HIFU) : technique non invasive plus récente, utilisant un faisceau d’ultrasons guidé par IRM.
Aujourd’hui, ces interventions occupent une place marginale dans la prise en charge de la maladie de Parkinson mais peuvent encore être envisagées dans certaines situations spécifiques, notamment chez les patients non éligibles à la SCP :
- Thalamotomie : pour un tremblement unilatéral réfractaire (maladie de Parkinson, tremblement essentiel)
- Pallidotomie : pour des dyskinésies sévères ou une rigidité prédominante non contrôlée par la médication
- Subthalamotomie (plus rare) : pour des symptômes asymétriques, dans des centres expérimentés.
Les chirurgies lésionnelles offrent des résultats rapides et souvent durable sur les symptômes ciblés. Cependant, leur efficacité reste limitée aux symptômes unilatéraux, l’intervention ne pouvant être réalisée que d’un seul côté en raison des effets secondaires importants d’une lésion bilatérale. Les troubles axiaux (marche, équilibre, parole) ne sont généralement pas améliorés.
Ces techniques présentent également plusieurs limites :
- Irréversibilité de la lésion (aucun ajustement possible ensuite, contrairement à la SCP).
- Risque de complications neurologiques : troubles de la parole, de la marche, de la motricité fine, voire déficit moteur ou cognitif, en cas de lésion trop étendue.
- Efficacité restreinte à un seul hémicorps, les lésions bilatérales exposent à des risques inacceptables.
- Radiochirurgie et HIFU : non invasives mais à effets différés, parfois incomplets.
Enfin, l’arrivée de techniques non invasives comme les ultrasons focalisés guidés par IRM pourrait relancer l’intérêt de ces approches dans un cadre plus sûr et plus ciblé.
Traitements chirurgicaux - SCP/DBS
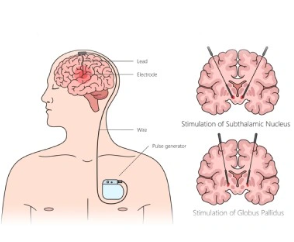
Stimulation Cérébrale Profonde (SCP)/Deep Brain Stimulation (DBS)Introduite dans les années 1980 et largement développée dans les années 1990, la Stimulation Cérébrale Profonde (SCP ou Deep Brain Stimulation–DBS) a révolutionné le traitement chirurgical des formes avancées de la maladie de Parkinson. Elle a progressivement supplanté les chirurgies lésionnelles, grâce à son caractère réversible et ajustable, permettant de moduler l’activité neuronale sans détruire les structures cérébrales.
La SCP est aujourd’hui le standard de référence pour le traitement des symptômes moteurs invalidants, des fluctuations et des dyskinésies dopaminergiques.
Cette intervention consiste à implanter une ou deux électrodes dans des structures cérébrales profondes ciblées, reliées à un neurostimulateur implanté sous la peau, généralement sous la clavicule.
Ces électrodes délivrent des impulsions électriques continues qui modulent l’activité des circuits moteurs, réduisant les symptômes sans provoquer de lésion permanente.
Le réglage des paramètres de stimulation (intensité, fréquence, durée de pulsation) peut être ajusté en fonction de l’évolution clinique du patient, offrant une grande flexibilité thérapeutique.Selon le profil clinique, la stimulation peut être bilatérale ou unilatérale, mais le plus souvent deux électrodes sont utilisées, une par hémisphère.
L’avancée des systèmes à stimulation adaptative permet de réguler automatiquement l’intensité de stimulation en réponse aux signaux neuronaux détectés (Local Field Potentials – LFP). Cette avancée permet d’adapter la stimulation aux fluctuations motrices, aux cycles de sommeil et aux prises médicamenteuses.
Selon les symptômes prédominants et le profil du patient, la SCP peut cibler différentes structures cérébrales profondes :
- le noyau sous-thalamique (NST), cible la plus courante, permet une amélioration globale des symptômes moteurs ainsi qu’une réduction de la dose de L-Dopa, particulièrement chez les patients présentant des fluctuations motrices et des dyskinésies
- le globus pallidus interne (GPi), souvent privilégiée chez les patients ayant des dyskinésies sévères ou chez les patients plus âgés, permet de réduire les dyskinésies tout en préservant la fonction cognitive.
- le noyau ventral intermédiaire du thalamus (VIM), principalement ciblé pour le contrôle du tremblement, notamment lorsqu’il est unilatéral ou dominant.
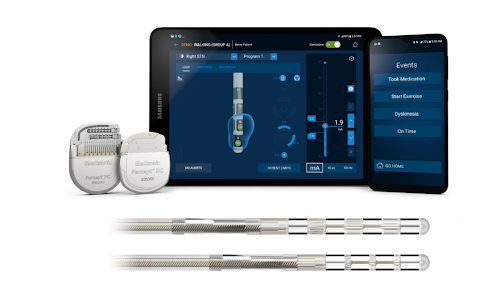
La SCP est indiquée pour les patients parkinsoniens présentant :
- Tremblement, rigidité ou akinésie non contrôlés par les médicaments
- Fluctuations motrices prolongées et dyskinésies sévères malgré un traitement optimal
- Parfois chez des patients plus jeunes pour préserver la vie professionnelle et sociale, ou pour limiter des effets secondaires psychocomportementaux de la dopathérapie
L’éligibilité repose sur une évaluation multidisciplinaire incluant neurologue, neurochirurgien, neuropsychologue, radiologue et infirmiers spécialisés. Elle est réservée à une fraction limitée des patients (10à15%) dont les symptômes restent invalidants malgré un traitement médicamenteux optimal.
La SCP entraîne une amélioration significative des symptômes moteurs dopa-sensibles dès les premiers jours suivant l’implantation. Elle réduit les dyskinésies et les fluctuations motrices, offrant une meilleure stabilité au quotidien. Elle permet également de diminuer la dose de L-Dopa, limitant certains effets secondaires liés au traitement médicamenteux.
Avec l’arrivée des systèmes à stimulation adaptative (aDBS), la thérapie devient dynamique et personnalisée, optimisant à la fois l’efficacité et la tolérance.Comme toute intervention invasive, la SCP comporte des risques chirurgicaux (hémorragie cérébrale, infection ou migration du matériel) et peut provoquer des effets secondaires liés à la stimulation (troubles de la parole, de la motricité fine, de l’humeur ou, plus rarement, cognitifs). La DBS n’améliore pas les troubles axiaux dopa-résistants (marche, équilibre, voix) ni certains symptômes non moteurs sévères. Cette technique nécessite également un suivi technique et neurologique régulier.
Physiothérapie
Exercices physiques (natation)
En ce qui concerne l’exercice physique, quelques remarques préliminaires sont nécessaires. Les mouvements sont essentiels à l’être humain. Une bonne hygiène de vie comprend notamment une activité physique régulière, nécessaire au bien-être général mais ayant également un effet bénéfique sur l’humeur, voire même sur certains symptômes somatiques dont la constipation. Le manque d’exercice entraîne un déconditionnement physique, un affaiblissement musculaire, des raideurs articulaires, voire des rétractions. Ceci est d’autant plus vrai que le patient est âgé.
Dans le cadre de la maladie de Parkinson, les patients présentent des difficultés motrices qui tendent à les isoler et dès lors, à réduire leurs activités physiques. Il est donc tout particulièrement important chez ces patients d’insister sur la nécessité de pratiquer une activité physique régulière, dans le but de garder une meilleure forme physique en général mais aussi de prendre une part active à leur traitement et de sortir de leur isolement.
Si le patient pratique régulièrement un ou plusieurs sports, il doit certainement être encouragé à poursuivre cette pratique. Le plaisir qu’il en tire lui est bénéfique, y compris sur le plan moteur, l’état thymique du patient pouvant avoir des répercussions directes sur ses symptômes moteurs.La natation est certainement un excellent sport en général. Elle favorise la coordination des mouvements et l’équilibre. Les mouvements réalisés dans l’eau nécessitent un effort réduit ; dès lors, certains exercices de mobilisation active peuvent être facilités. Les bienfaits peuvent être ressentis pendant plusieurs heures. Chez les patients plus évolués, la température de l’eau devrait idéalement se situer entre 28°C et 30°C. Les patients confrontés au problème des fluctuations motrices doivent toujours être accompagnés dans l’eau puisqu’ils peuvent se trouver en difficulté à l’improviste.
L’exercice physique doit être pratiqué régulièrement, en principe quotidiennement. Des séances fréquentes, même si elles sont courtes et représentent un effort modéré, sont préférables à des séances occasionnelles d’intensité exagérée, trop fatigantes. L’exercice doit concerner le corps entier mais également parfois des régions plus spécialement impliquées dans les difficultés particulières des patients. Les instructions initiales du kinésithérapeute sont utiles. Certains patients, surtout pendant les premières années, pourront ensuite reproduire ces exercices seuls à domicile.La kinésithérapie
A des stades plus avancés de l’affection ou chez des patients plus âgés, ou lorsque les troubles posturaux avec risque de chute sont importants, l’aide systématique du kinésithérapeute peut s’avérer utile. Une kinésithérapie de rééducation individuelle est souvent nécessaire, en tout cas chez les patients qui présentent une symptomatologie akinéto¬hypertonique nette. Elle devient indispensable lorsqu’il existe des fluctuations motrices et plus encore, lorsque le trouble de la marche ou les troubles posturaux sont à l’avant-plan.
Des massages peuvent être utiles par leur effet sur la tension musculaire. Néanmoins, en sus de ceux-ci, il est important de réaliser une mobilisation active et / ou passive des principales articulations (épaules, hanches) dans le but de prévenir ou de lutter contre les rétractions articulaires et tendineuses. Enfin, des exercices d’équilibre et de marche, en insistant sur le rythme, paraissent incontournables.
Les exercices de groupe peuvent convenir aux patients modérément symptomatiques. Il s’agit d’un choix individuel.En Belgique, les patients atteints de la maladie de Parkinson peuvent bénéficier, sur demande d’un neurologue, d’un remboursement de la kinésithérapie en pathologie lourde jusqu’à une séance quotidienne.
Une règle à suivre pour tous les patients : ne pas vouloir se surpasser lors des exercices mais travailler de sorte que ceux-ci procurent une sensation de bien-être général à la fin de la séance.
Une cassette concernant des exercices à pratiquer chez soi peut être obtenue au siège de l’Association Parkinson Francophone.
L’ergothérapie
L’ergothérapie trouve sa place dans une perspective fonctionnelle. Elle a pour but d’améliorer les fonctions motrices et mentales, en faisant appel à un travail spécifique en rapport avec les activités de la vie quotidienne. On parvient à corriger un mouvement pathologique en invitant le patient à accomplir des gestes nécessitant l’exécution du mouvement affecté. L’important n’est pas tant ce que le patient fait mais bien la façon dont les mouvements requis sont exécutés.
En outre, durant les séances d’ergothérapie, le patient peut s’entraîner à réaliser des activités quotidiennes qui lui posent des difficultés : écrire, se servir de ses couverts, manipuler une clé, écrire.
Enfin, on conseillera au patient l’usage d’objets adaptés à ses difficultés. Par exemple, un stylo plus gros ou des gadgets que l’on place autour de son crayon, permettant une meilleure prise, facilitent souvent l’écriture.La logopédie
La logopédie prend en charge les difficultés motrices de la sphère oro¬pharyngo-laryngée. Elle peut donc être indiquée dans les troubles de l’articulation et de la phonation mais aussi dans les troubles de la déglutition. Si l’on veut que les exercices d’élocution soient efficaces, il convient de s’y astreindre consciencieusement et régulièrement. Il est parfois aussi utile de s’entraîner simplement à lire un texte à haute voix sous la supervision d’un membre de l’entourage. Ici encore, la cassette d’exercices disponible auprès de l’Association peut aider les patients. Les troubles de déglutition nécessitent plus volontiers l’aide d’un professionnel.
